李益民教授|金属注射成型制备NiTI血管支架的技术探索
导读▏获得低杂质零件对于成功制备MIM NiTi支架至关重要。中南大学李益民博士、舒畅博士通过金属注射成型(MIM)获得了低氧含量为0.17%的MIM NiTi合金和支架,并评估了多项性能。本研究为镍钛自膨胀血管支架提供了一种新的制造策略。此外,研究旨在利用MIM工艺的特点开发多孔和梯度多孔NiTi血管支架。
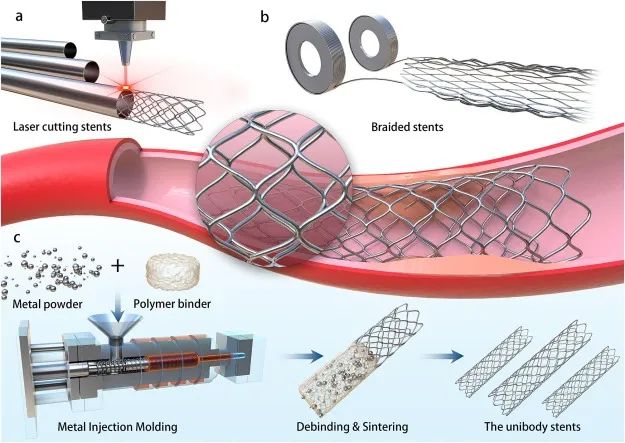
图1. 血管支架生产工艺示意图:(a)激光切割,(b)编织法,(c)金属注射成型。
以Ni:Ti原子比为50.49:49.51的球形预合金NiTi粉末(D50=10.9μm)为原料。粘合剂组合物为60%石蜡(PW)、38%聚丙烯(PP)和2%表面活性剂硬脂酸(SA)。粉末装载量设计为65%。混合过程在高纯度氩气(99.999%)的保护下进行。混合在160-180°C下进行3小时,根据实际扭矩变化进行调整。原料通过注塑机成型。调整注射的压力和温度,以确保没有裂纹和气泡等缺陷。溶剂脱脂在二氯甲烷中于38°C下进行12小时。样品在真空烧结炉中用钼加热器在钼板上烧结。最高烧结温度为1240°C(保持6小时)。在10-4Pa和10-2Pa的真空条件下,分别获得了含0.17和0.37wt%氧气的样品。NiTi合金的碳含量低于0.05wt%。绿色、溶剂脱粘和烧结零件如图2a所示。通过线放电加工切割线(图2b)和盘(图2c)样品进行生物相容性测试。低氧镍钛合金用于制备支架样品(图2d)。支架支柱的厚度约为180μm(图2f)。支架长度和直径的收缩率分别约为1.13和1.14。

图2. MIM NiTi材料和支架。(a) 注塑生坯、溶剂脱脂和烧结零件。(b) 电线样品。(c) 光盘样本。(d–g)支架产品原型的形态。
对MIM NiTi合金的材料性能进行了评估,包括拉伸性能、微观结构和马氏体相变行为。MIM NiTi合金在室温下的拉伸性能如图3所示。MIM具有很高的氧化风险,氧含量对机械性能有很大影响(图3a)。低真空烧结(10-2Pa)产生0.37%的氧气,导致抗拉强度为432MPa,伸长率为2.3%。在10-4Pa的高真空压力下,0.17%氧气的存在使拉伸强度提高到812MPa,伸长率提高到5.7%。氧含量的增加促进了脆性Ti4Ni2O的形成,这对合金的机械性能有害。通过DIC检查了整个变形过程中的应变分布。如图3b和c所示,在5%的拉伸加载和卸载实验中,MIM NiTi合金的应变分布相对均匀。拉伸卸载后,约有3%的残余应变仍然存在。通过用外部加热装置在120°C下加热,样品在很短的时间内完全回收。MIM NiTi合金在5%预应变下表现出优异的恢复性能。镍钛合金的恢复性能对血管支架的顺应性和抗疲劳性至关重要。将对使用低氧工艺制备的MIM NiTi合金进行进一步分析和支架制备。
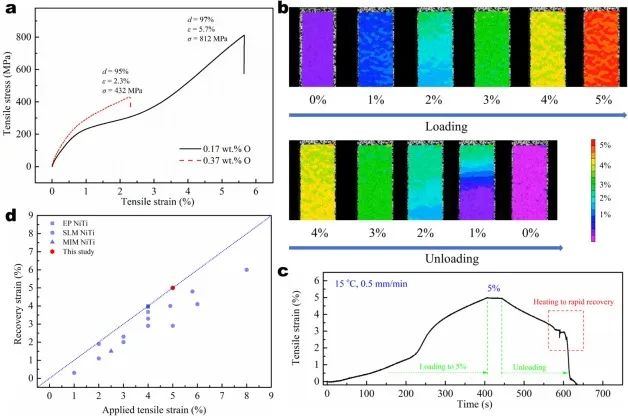
图3. 室温(15°C)下的拉伸和恢复性能。(a–b)加载和卸载过程中5%拉伸应变的DIC分析。(c) 拉伸应力-应变曲线。
值得注意的是,尽管在5%的应变下实现了完全恢复,但在5.66%的应变下立即发生了断裂。通常,当应变超过8%甚至10%时,NiTi合金开始滑动并进入塑性变形。这表明NiTi合金的正常塑性变形可能无法有效触发,可能是由于沉淀对滑移应力的强化作用或基体韧性不足。进一步的研究可以集中在提高基体韧性或消除不均匀的Ni4Ti3沉淀上,以应对这些挑战。
图4a显示了背散射模式下的SEM形态,显示了除NiTi基体外的少量残余孔隙和Ti2Ni夹杂物。放大图像中可以看到粗大的Ni4Ti3沉淀物。金相腐蚀处理后(图4b),晶界和高能沉淀物优先腐蚀,留下凹坑,如报告所述。
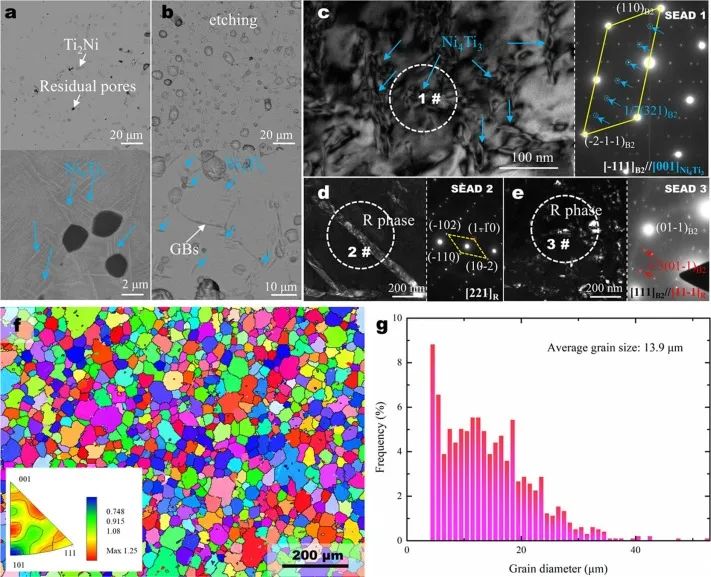
图4. MIM NiTi合金的微观结构。扫描电镜形态(a)蚀刻处理前和(b)蚀刻处理后。(c–e)相组成的透射电子显微镜分析,包括亮场和暗场图像以及SAED。(f) EBSD分析的IPF图。纹理系数的最大值为1.25。(g) 粒度分布。
Ti2Ni主要沿晶界分布。由于热脱脂和烧结过程,这些边界更容易受到氧化污染。氧使Ti2Ni稳定,形成具有核壳结构的Ti4Ni2O。先前的研究表明,通过密度泛函理论计算,Ti4Ni2O中的氧与间隙位置的氧相比具有较低的自由能。同时,增加NiTi合金中的标称Ti含量会导致Ti2Ni(包括Ti4Ni2O)的增加。微米级Ti2Ni与基体没有非相干关系。Ti2Ni含量越高,裂纹源越多,断裂韧性越低。在制备过程中,Ti2Ni的形成导致基体中的Ti耗尽,从而导致转变温度整体降低。同时,Ni在局部畴中富集,这是形成Ni4Ti3沉淀物的前兆。在MIM NiTi合金中,即使没有特定的时效处理,烧结过程中也会发生不均匀的Ni4Ti3沉淀。图4b显示,粗大的Ni4Ti3沉淀物主要沿着Ti2Ni旁边的晶界分布。
纳米尺寸的Ni4Ti3沉淀物也存在于基体中。如图4c-e所示,Ni4Ti5沉淀物和R中间相可以在TEM亮场图像和选区电子衍射(SAED)中找到。Ni4Ti3周围的非均匀应力场有助于从B2-B19′到B2-R-B19′的两步相变。在Ni4Ti3分布不均匀的情况下,也可能发生三步或四步相变。
MIM NiTi合金的EBSD分析结果如图4f所示。逆相位图(IPF)图显示最大纹理指数为1.25,没有主导取向,这有利于稳定获取力学性能。图3g所示的粒度分布显示平均粒度为13.9μm。
使用DSC研究了MIM NiTi合金的转变温度。如图5a所示,冷却过程显示出加宽的R峰和马氏体峰(B2-B19',R-B19')。加热过程显示奥氏体转变(B19′-B2)。R峰值(Rp)温度为38°C,马氏体峰值(Mp)为-19°C,奥氏体峰值(Ap)为39°C。热滞宽度为58°C。R相和B19′相的潜热分别为27.4和10.9 J/g,总值为38.3 J/g。B2的相变潜热为31.5 J/g。图5b显示了MIM NiTi合金在10个DSC循环中的循环稳定性;Ap和Mp的位移值如图5c所示,最大位移为0.6°C。
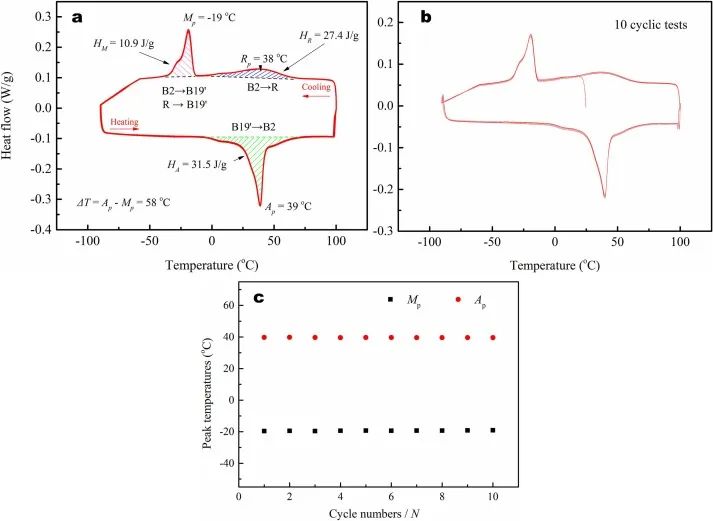
图5. (a) 差示扫描量热法(DSC)曲线和相变参数:马氏体峰值温度(Mp)、奥氏体峰值温度(Ap)、R相变峰值温度(Rp)、潜热(HR、HA、HM)和热滞后(ΔT)。(b) DSC测试的十个周期。(c) 热循环试验转变温度的变化值。
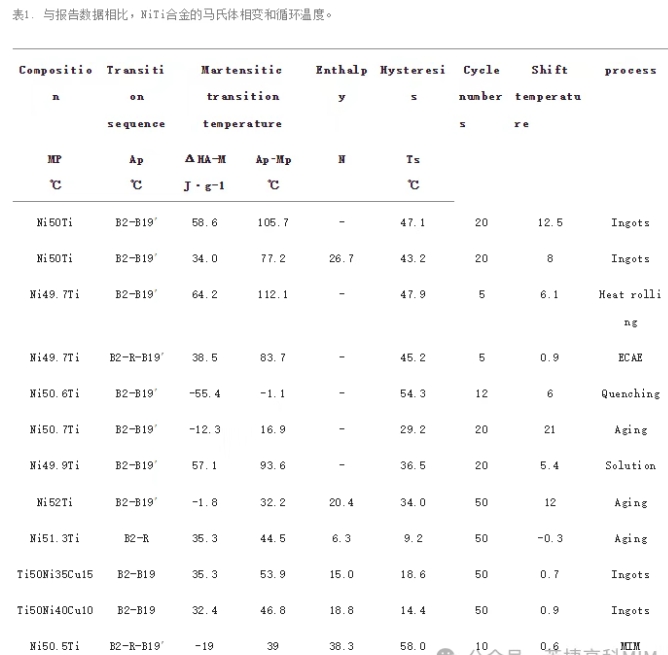
表1显示了常见铸造NiTi合金的相变温度、相变顺序和循环性能。MIM NiTi合金表现出极宽的热滞后和相当低的循环偏移。这种行为归因于烧结MIM NiTi合金中存在不均匀的Ni4Ti3沉淀。细小的Ni4Ti3沉淀物对相界具有钉扎效应,增加了相变阻力。此外,这些沉淀物可以增强位错的临界滑移应力,从而减少热循环过程中位错的产生,这有利于保持热循环稳定性。不同尺度的非均匀Ni4Ti3沉淀物的同时存在有助于在这些合金中观察到的R峰变宽。
如图6所示,对MIM NiTi合金的应力循环稳定性进行了评估。由于室温下多相共存,试验在75°C下进行,以排除R相和马氏体的干扰。
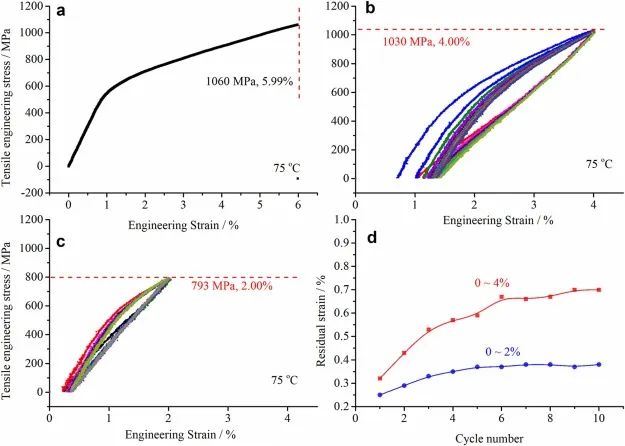
图6. 75°C(>Af)下拉伸加载-卸载过程中的循环稳定性。(a) 75°C下的工程应力-应变曲线。(b,c)分别在4%和2%的最大应变下绘制10个循环的拉伸应力-应变曲线。(d) 恢复后的残余应变行为。
在完全奥氏体状态下,观察到更高的抗拉强度和相似的伸长率。与15°C下的试验结果相比(图3a),强度从812 MPa增加到1060 MPa。伸长率仍不超过6%。这种特殊现象需要仔细研究。
一种可能的机制是:B19′马氏体的拉伸过程涉及去孪晶、塑性变形和断裂。B2奥氏体的拉伸过程涉及应力诱导马氏体相变、塑性变形和断裂。尽管B2和B19′在最终断裂前具有相同的结构和相似的理论强度,但塑性变形中晶粒的协调和多晶NiTi中B19′的脱嵌可能会导致更多的裂纹源(与全B2状态相比)。在MIM NiTi合金中,与铸锭冶金NiTi合金相比,由于高水平的裂纹源(包括残余孔隙率、Ti4Ni2O和粗Ni4Ti3),裂纹在引发位错滑移之前已经膨胀并开裂。因此,在全B2状态下获得了更高的强度。
4%和2%应变下的循环试验如图6b和c所示。残余应变逐渐增加并趋于稳定值。可以看出,MIM NiTi具有更好的超弹性和稳定性。热循环稳定性和应力循环稳定性为血管支架的高抗疲劳性提供了基础。
在测试过程中,使用PBS对管腔内血管支架进行受控管腔压力调节,通过周期性膨胀和收缩模拟血管内支架力的变化。模拟血管的管腔压力控制方案如图7a所示。加速疲劳试验以50Hz的频率进行,整个过程持续约2197.3小时。
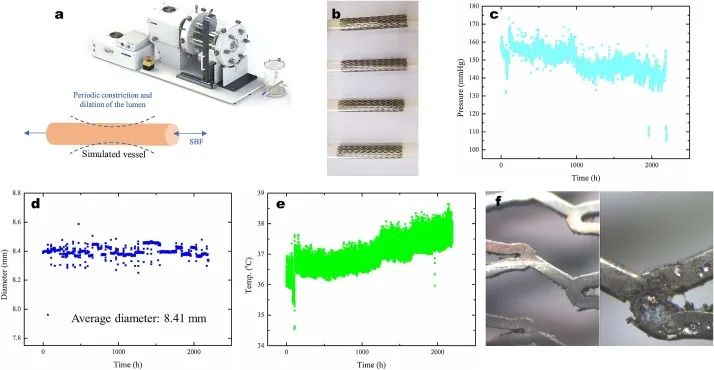
图7. (a) 血管支架体外疲劳试验机和方法。(b) 模拟血管中的支架。(c–e)疲劳试验期间支架压力、直径和温度的变化(循环次数:3.96×108)。(f) 疲劳试验后NiTi支架的表面形态。
每10分钟记录一次模拟血管系统的参数,在整个过程中捕获数据,包括管腔内压力、支架直径和管腔内温度(图7a-c)。在测试过程中,压力超过了安全的人体血压水平,平均为149 mmHg,相当于硅胶模拟血管外径的平均应变为0.87%,相应支架加载区域(硅胶管内径)的平均应变不小于1.07%。平均测试温度为36.97°C,在该温度下,血管支架的平均直径为8.41 mm,在2197.3小时的测试持续时间内,在平均值附近波动。这可以归因于MIM NiTi合金在测试温度下具有优异的超弹性,这使得支架能够在长时间使用后保持设计的外径而不会降低其支撑功能,从而确保稳定的机械可靠性。
如图8a和b所示,对HUVEC进行的增殖毒性试验(CCK-8)显示,用EGM-2培养的细胞存活率为100%(对照组),而用EGM-2中制备的NiTi金属100%浸出液培养的HUVEC存活率为81.2±3.8%(实验组),差异具有统计学意义(t=12.188,P<0.001)。从MIM NiTi合金制备的提取物没有明显的细胞毒性(存活率>70%)。图8显示了在NiTi合金板表面培养1-3天的HUVEC的细胞形态。SEM图像显示,HUVEC很好地粘附在NiTi合金板上,显示出健康的形态,呈纺锤形或多边形。观察到丝状和板状伪足,突出了生物细胞对MIM NiTi合金的亲和力。
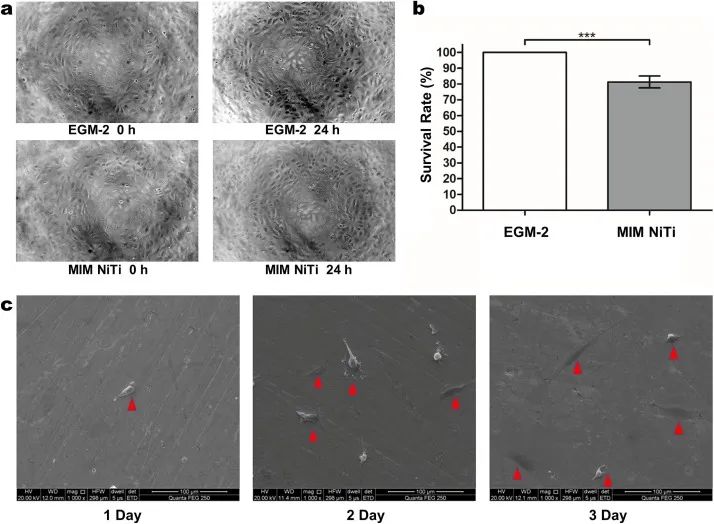
图8. (a) 在光学显微镜下,对人脐静脉内皮细胞(HUVEC)在EGM-2和NiTi金属100%浸出液中孵育0和24小时后的生长进行形态学比较(×100)。(b) CCK-8法检测镍钛金属100%渗滤液对HUVEC存活率的影响。N=6,***与对照组相比,P<0.001。(c) SEM检测共培养1、2和3天的NiTi合金片中HUVEC的细胞粘附形态。
实验组和对照组的内皮HUVEC在低营养环境中培养,几乎没有增殖,以检查细胞的运动和迁移。通过刮擦细胞单层(0小时)去除细胞的确定区域,并继续培养24小时。观察到细胞向中间清除区域的迁移行为,如图9a所示。对清除区面积的变化进行量化,以确定细胞迁移率,详细的迁移率数据如表2所示。
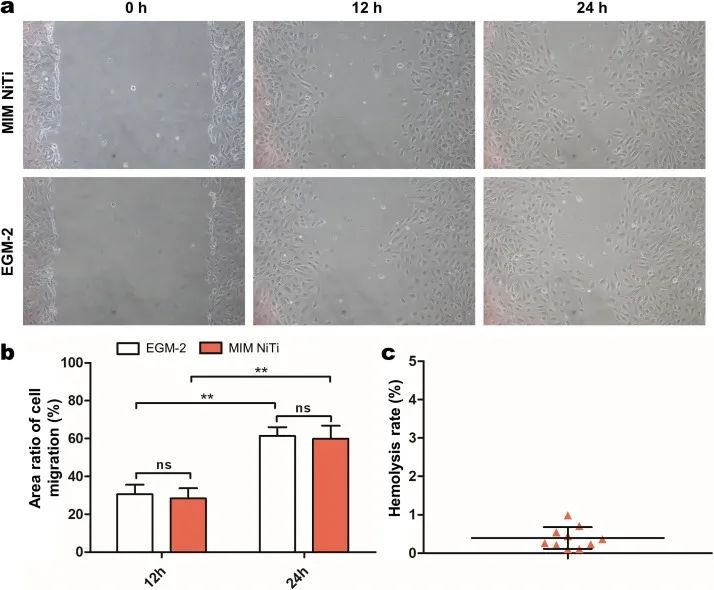
图9. (a) 细胞迁移试验在缺乏增殖的低营养条件下进行。(b) 12和24小时细胞迁移的面积比,**表示P<0.01,ns表示P>0.05。(c) 10名不同的成年健康志愿者(人类血液)在MIM NiTi合金上的溶血率。
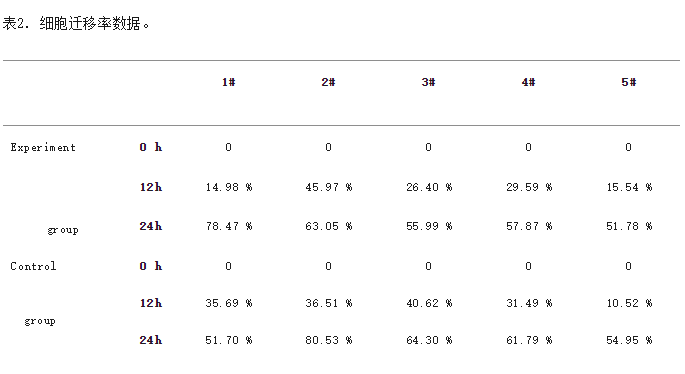
图9b显示了细胞迁移的平均面积比以及实验组和对照组之间的统计差异。其中,两组在12小时和24小时的迁移率均显著增加。然而,在相同的孵育时间下,对照组和实验组之间的比较结果P>0.05,表明没有显著的统计学差异,这表明MIM NiTi合金没有显著抑制细胞迁移。这些发现表明,MIM NiTi合金血管支架对血管内皮化过程没有显著的抑制作用,这有利于内皮层的修复和局部支架环境的稳定(表3)。

图9c显示了MIM NiTi合金的溶血率(人体血液)。Zhang等人研究了使用兔血作为介质的激光梯度润湿处理前后的溶血率,并观察到溶血率从1.32%降低到0.94%;Cheng等人激光加工了特定的NiTi表面微观结构,将羊血的溶血率从4.69%降低到1.56%。这表明NiTi表面本身的微观结构对血液相容性有显著影响,F.Mohammadi等人通过阳极氧化和壳聚糖-肝素纳米粒子涂层的组合共同验证了这一点,显著降低了NiTi合金对人体血液的溶血率,从最初的3.4%降至0.9%。通过测试大量测试样品对本研究中使用的MIM NiTi合金进行了评估,并实现了0.4%的相当低的溶血率,这归因于MIM NiTi铝合金本身的表面性能。NiTi合金中的Ni2+在引发凝血方面起着关键作用,较低的Ni2+释放率将导致优异的血液相容性。MIM NiTi合金与铸锭NiTi合金相比具有更高的氧含量,特别是界面氧含量,这促进了TiO2保护层的形成并增强了生物相容性。
本研究提出金属注射成型作为镍钛血管支架的制备技术,可以大大减少加工过程。MIM工艺容易氧化。严格控制并获得较低氧含量的NiTi合金具有较高的机械性能。最小氧含量为0.17 wt%的MIM NiTi合金对应于812 MPa的抗拉强度和5.7%的伸长率。它的恢复应变为5%。在3.96×108循环模拟体外疲劳试验中,MIM NiTi合金基本上保持了恒定的直径,没有任何明显的损伤,尽管观察到局部点蚀。基于人脐静脉内皮细胞的毒性、迁移和粘附,评估了MIM NiTi的生物相容性。溶血率低至0.4%。MIM NiTi支架展现出卓越的支撑性能和生物相容性。
李益民教授简介

李益民,中南大学粉末冶金研究院二级教授、博士生导师。国家万人计划科技创业领军人才、教育部新世纪优秀人才、国家科学技术进步奖、中国青年科技奖获得者;全国百篇优秀博士论文、全国优秀博士后获得者、英捷高科创始人。长期从事粉末冶金先进成形技术及材料、医用生物材料等的研究与开发工作,提出了粘结剂辅助成形工艺中伴随粘结剂脱除的前致密化过程、高精度粉末注射成形技术、脱脂临界厚度等创新学术概念,出版国内第一本金属注射成形原理的学术专著,授权国家专利100余项,发表论文超400篇。

 中文
中文
 英文
英文






